Votre panier est actuellement vide !
L’IDENTIFICATION DES INTERACTIONS PROTÉINE-PROTÉINE
Purification par affinité couplée à la spectrométrie de masse (APMS)
Identifier et quantifier les partenaires d’interaction de votre protéine d’intérêt. L’époque où l’on découpait une bande dans un gel pour identifier un partenaire d’interaction est révolue.
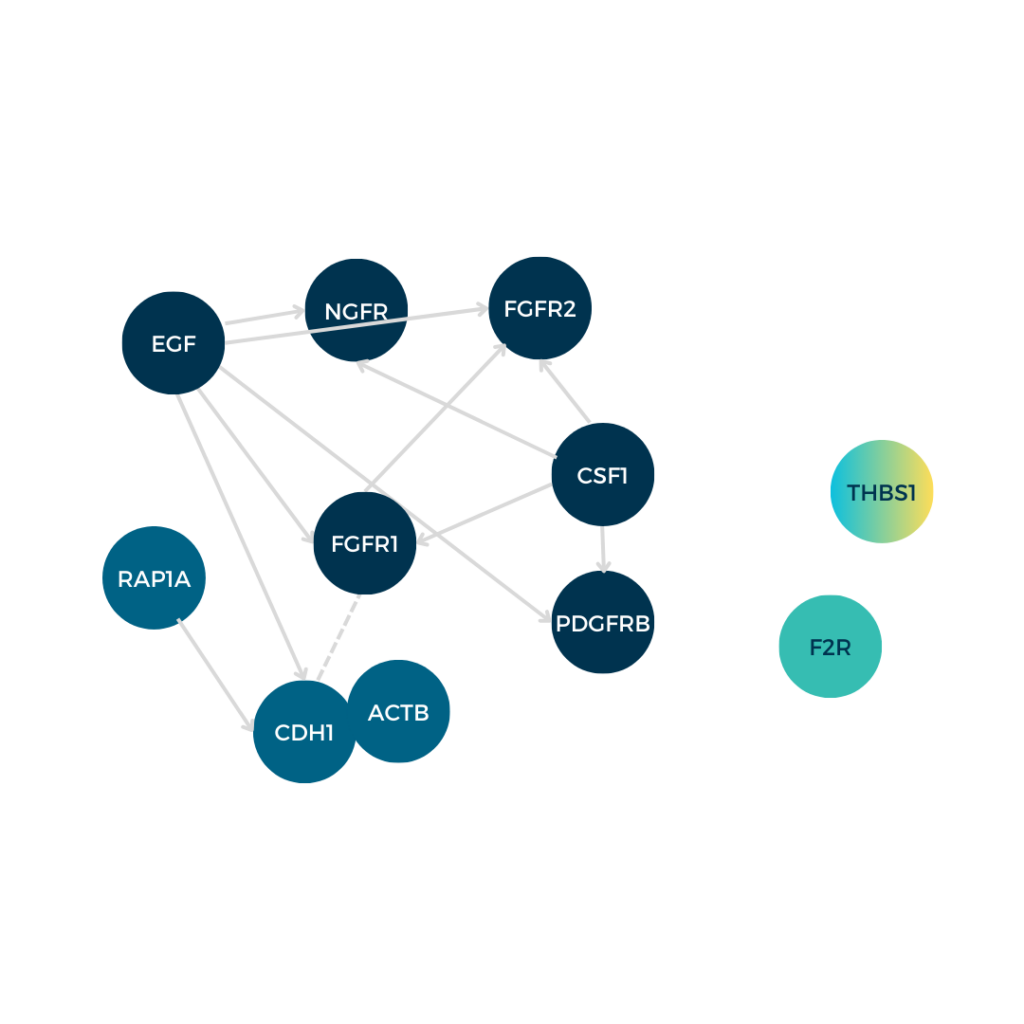
Solutions APMS
Avez-vous besoin de plus qu’une simple liste de protéines ?
L’utilisation de méthodes de purification par affinité telles que l’immunoprécipitation permet d’isoler des complexes protéiques entiers à partir d’un extrait de cellule ou de tissu. Autrefois, ou lorsque la connaissance de l’identité d’une seule protéine était nécessaire, les protéines immunoprécipitées étaient résolues par SDS-PAGE, colorées, et les bandes individuelles étaient coupées et analysées par LC-MS/MS. Avec les instruments modernes, le complexe protéique entier peut être soumis à une digestion protéolytique et analysé par LC-MS/MS. Le résultat d’une telle expérience est une liste de protéines qui ont été co-immunoprécipitées avec l’appât.
Il est intéressant de noter que notre workflow APMS est compatible avec la protéomique quantitative sans étiquette. Par conséquent, si nécessaire, nous pouvons fournir des informations quantitatives sur chaque protéine IPed par rapport à une condition de contrôle. Cette expérience est idéale pour comparer l’affinité des partenaires d’interaction avec votre protéine d’intérêt dans deux conditions ou plus.
Capacités connexes
Protéomique
Obtenez des données quantitatives pour jusqu’à 6500 protéines dans vos échantillons grâce à notre workflow de protéomique quantitative sans étiquette.
Métabolomique
Des workflows optimisés et éprouvés en spectrométrie de masse pour analyser, caractériser ou identifier les protéines.
Lipidomique
Obtenez un profilage approfondi de nombreuses classes de lipides biologiquement importants grâce à nos instruments à haute résolution.
Analyse de données
Nous aidons nos clients à exploiter la valeur et le potentiel de leurs données en leur fournissant des informations plus claires et plus approfondies.
Entrez en contact
Communiquez avec nos experts
